| 일 | 월 | 화 | 수 | 목 | 금 | 토 |
|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 8 | 9 | 10 | 11 | 12 | 13 | 14 |
| 15 | 16 | 17 | 18 | 19 | 20 | 21 |
| 22 | 23 | 24 | 25 | 26 | 27 | 28 |
| 29 | 30 | 31 |
- 핀트
- 핀트 수익률
- 핀트 투자
- 성남 야외 농구장
- 주린이
- 삼전우
- 오블완
- 핀트 마이너스
- 티스토리챌린지
- 성남 농구장
- 실내 농구장
- 기업은행 주가
- 삼전 모으기
- 공모주
- 주식
- 용인 농구장
- 삼성전자 배당금
- 삼성
- 대한항공
- 의료기기 밸리데이션
- K3 엔진오일
- 주식일기
- 삼전
- 삼성전자
- 기업은행 주식
- 삼성전자 모으기
- 삼성전자우
- 삼전우 모으기
- 경기도 광주 농구
- 삼성전자우 모으기
- Today
- Total
갱얼쥐
의료기기&제약 클린룸 등급에 따른 미생물 관리 기준 (feat. 국가별 미생물 관리 기준) 본문
이전 글에서 클린룸 입자 수에 따른 등급 판정 방법에 대해 공부했다.
의료기기&제약 클린룸 입자 수에 따른 등급 판정 방법 (feat. 클린룸 밸리데이션 준비, 입자 계수
의료기기 및 의약품을 만들거나 다룰 때 무균 환경은 필수이다. 의료기기의 경우, 인체에 삽입되어 사용되는 경우(보통 4등급)는 클린룸의 필요성이 더욱 두드러진다. 의약품의 경우, 건강과 직
0606.tistory.com
클린룸의 청정도를 유지하기 위해서는 일반적으로 Particle, 온습도, 차압, 조도, 부유균, 낙하균, 표면균, 작업자 손끝 세균, 멸균 전 생균수(바이오버든) 등을 관리해야한다.
이번에는 클린룸 등급에 따른 미생물 관리 기준을 알아보려고 한다.
여기서 말하는 미생물은 바이러스, 박테리아, 진균, 원생생물(조류, 원생동물)로 나뉜다.
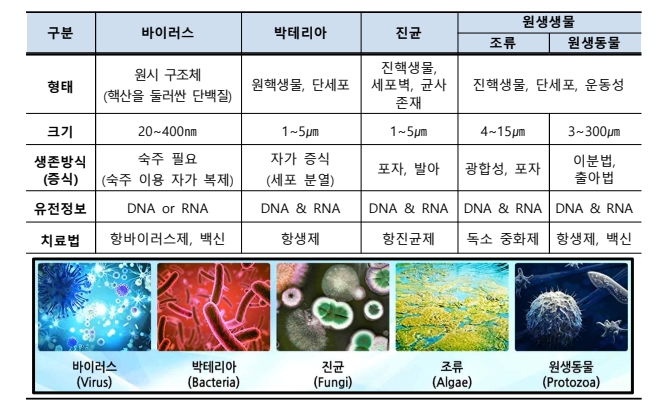
의료기기의 경우 공기, 작업자, 작업대, 장비 등에서 박테리아(세균)과 진균(곰팡이)를 측정하여 미생물 오염도를 판정한다.
클린룸 등급에 따른 미생물 관리 기준(ISO, KGMP, FED STD, EU GMP, cGMP)
1. ISO(International Organization for Standardization) : 발행된 규정 중 ISO 14698에 미생물 오염에 관한 일반적인 지침이 담겨있다.
위 규정에 따르면 미생물 관리를 위한 품질 시스템 설정을 위해 아래와 같은 사항을 요구하고 있다.
- 미생물학적 관점에서 경계, 조치 및 목표 수준 설정
- 설정된 주기로 지속적인 모니터링
- 미생물 오염 검출 및 모니터링은 샘플링 계획에 따라 적절한 방법으로 실시
* 증식 위험이 있는 지역에서 모니터링(준공 및 비운전 상태), 일상 모니터링(운전 상태)
- 청정실 내 상황의 복잡성과 다양성을 반영하여 샘플링 실시
* 샘플링 계획 시 청정실은 운전상태이며, 최대 활동량이 발생했을 때 실시
- 샘플 배양 시 예상되는 미생물의 유형에 따라 배지 및 배양 조건 선택
* 배지는 다른 지시 사항이 없는 경우 비선택적
* 배양 기간 : 박테리아(2~5일), 곰팡이(5~7일)
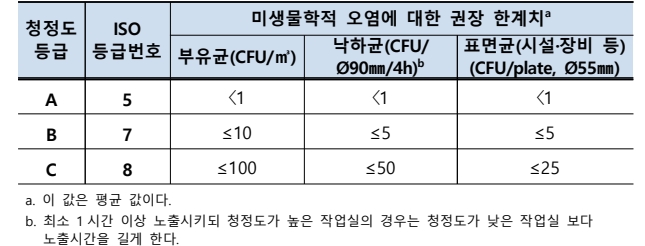
2. KGMP(Korea Good Manufacturing Practice) : 말그대로 대한민국 GMP이다. ISO 규격을 따라가는 추세이기에 ISO 규정과 같다고 보면 된다. 위 표로 첨부한 의료기기 제조시설 청정도 관리 가이드라인 또한 ISO 규정을 참고하여 만든 것이다.
3. FED STD(Fedral Standard) : 미국 연방 표준이다. 이 규정에는 미생물 관리에 대한 내용이 없다. 과거에는 주로 사용되던 규정이었는데, 현재 시대에 맞지 않아 사용되지 않고 있다.
4. EU GMP(European union Good Manufacturing Practice) : 유럽연합 GMP이다. 이것 또한 ISO 규정을 참고하여 작성되었기 때문에 위 표 기준을 참고하면 된다.
5. cGMP(Current Good Manufacturing Practice) : 현행 우수 의약품 제조 및 품질 관리 기준으로 미국 FDA에서 정한 규정이다.
부유입자도 같이 포함되어 있다.
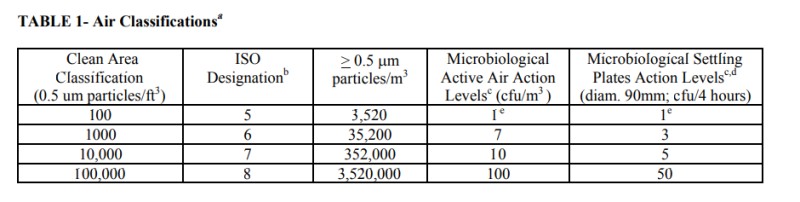
정리하자면 분류를 두가지로 나눌 수 있다.
- ISO, KGMP, EU GMP : ISO 기준 따름
- cGMP : 미국 FDA 기준을 따름
미생물 측정을 위한 장비
미생물은 어떻게 측정해야 할까?
장비는 Air Sampler가 있고, 채취한 미생물을 배양하기 위한 배지 및 Incubator가 필요할 것이다.
- Air Sampler(부유균 측정기)
여러 회사의 장비가 있다. 가장 유명한 곳으로는 VWR이라는 회사 제품인 SAS 모델일 것이다. 열에 아홉은 이 회사 제품을 사용하고 있을 것이라고 생각한다. 외에도 머크, MICRONVIEW 등 다른 회사들도 있긴하다.

에어 샘플러에 배지를 장착해서 작동시키면 끝이다.
채취 시간, 위치 등은 사용자가 설정하기 나름이지만, 대략적인 가이드라인이 있긴하다.
* KGMP : 의료기기 제조시설 청정도 가이드라인 참고할 것
- 배지 : 미생물, 세포, 조직 등을 인공적으로 배양하여 증식시키기 위한 영양원
타겟하는 미생물에 따라 배지가 달라진다.
총 부유균 측정 시 사용되는 배지
TSA(TRyptic Soy Agar): 가장 일반적으로 사용, 다양한 종류의 세균이 자랄 수 있는 영양분 함유
PCA(Plate Count Agar): 다양한 세균 성장 가능 (주로 식품 산업에서 사용)
특정 균종 측정 시 사용되는 배지
MAC (MacConkey Agar): 대장균군과 같은 그람 음성균, 특히 유당을 발효하는 균
EMB (Eosin Methylene Blue Agar): 대장균군의 분리 배양에 사용
MSA (Mannitol Salt Agar): 황색포도상구균과 같은 호염성 세균
SDA (Sabouraud Dextrose Agar): 곰팡이와 효모
BCYE (Buffered Charcoal Yeast Extract Agar): 레지오넬라균 등

에어 샘플링한 배지를 Incubator에 넣어 배양 시키면 Colony가 생성되는데, 그 Colony를 관찰하여 미생물 오염도를 평가한다.
에어 샘플링이 필요 없는 손끝 균 등은 배지에 손을 얹어 오염 시킨다던지 하는 방법으로 측정한다.
오늘 공부의 결론은 의료기기 산업은 ISO 기준까지만 따라도 충분할 것이고, 제약 산업도 ISO 기준으로 충분하다고 볼 수 있지만, 미국 진출을 노린다면 cGMP 기준도 충족해야 한다라는 의미로 해석할 수 있다.
우리 회사가 타겟으로 삼는 국가를 기준으로 관리를 하는 것이 정답인 것 같다.
아래 규정들은 클린룸 관련 내용으로 한번 봐두면 좋을 것 같은 규정들이다.
어디서 어떻게 구할지 모르는 사람들을 위해 업로드해본다.
끝!
'업무 > 품질관리' 카테고리의 다른 글
| 의료기기 멸균 밸리데이션 관련 (feat. 필러 의료기기 멸균 종류) (0) | 2024.11.25 |
|---|---|
| 의료기기 위험관리에 대하여 (feat. 위험관리 작성 방법) (1) | 2024.11.24 |
| 의료기기&제약 국가별 품질문서 체계 관련 (1) | 2024.11.22 |
| 의료기기&제약 클린룸 밸리데이션 관련 (feat. 의료기기 밸리데이션 위주) (1) | 2024.11.21 |
| 의료기기&제약 클린룸 입자 수에 따른 등급 판정 방법 (feat. 클린룸 밸리데이션 준비, 입자 계수기(Particle counter) 브랜드) (0) | 2024.11.19 |



